この治験は肝硬変の患者さまの肝臓の線維化を改善し、 肝機能を回復させることを期待して開発中のお薬の、
有効性と安全性を確認することを目的に実施されます。B型・C型肝炎、非アルコール性脂肪肝炎(NASH)により
肝硬変になった患者さまのご協力が必要です。治験参加のご検討をお願いいたします。
0120-800-739
【受付時間】平日9:00~17:00(土・日・祝日・年末年始を除く)
治験
対象:18歳~79歳の男女
B型肝炎、C型肝炎、非アルコール性脂肪肝炎(NASH)による肝硬変と診断された方
 大原薬品工業株式会社
大原薬品工業株式会社
肝硬変で線維化してしまった肝臓を改善させる目的で開発中のお薬の治験に、ご協力をお願いいたします。
肝硬変で線維化してしまった肝臓を改善するお薬の開発が始まっています。
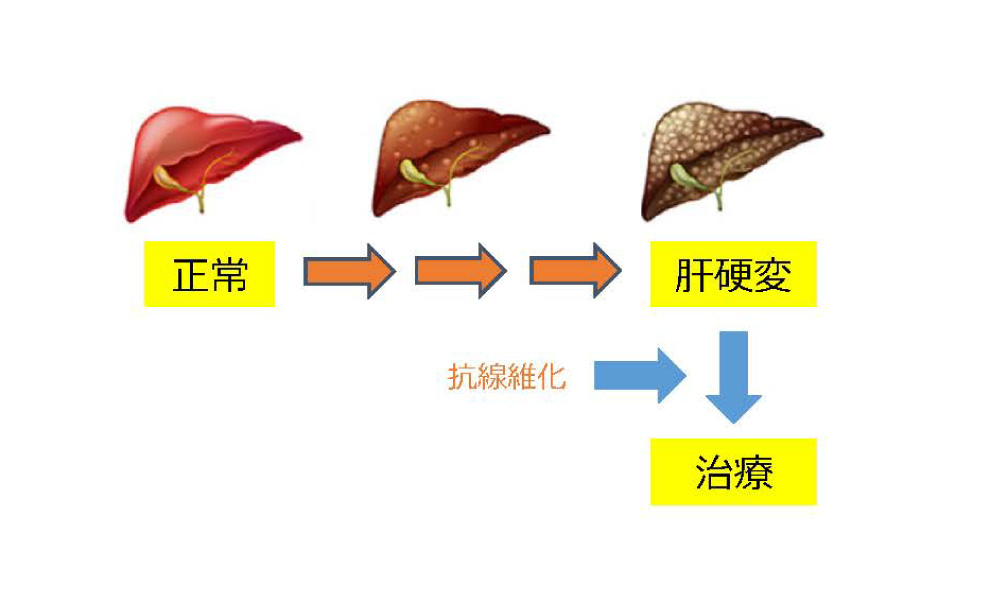
主な参加条件
- 18歳~79歳でB型肝炎、C型肝炎、非アルコール性脂肪肝炎(NASH)による肝硬変と診断された方
※非アルコール性脂肪肝炎(NASH)による肝硬変の方は、参加者が集まったため、募集を終了とさせていただきました。皆様、ご協力の程、ありがとうございました。
- 最寄りの治験実施医療機関に週2回(点滴時間:3~4時間)計24週間の通院ができる方
- Child-Pugh分類がグレードB(中等度:7~9点)の方(わからなくてもご応募いただけます)
- かかりつけ医から、診療情報提供書を発行していただける方
※今回の治験では肝硬変の原因がB型肝炎、C型肝炎、非アルコール性脂肪肝炎(NASH)であると診断された方に限定させていただいております。
非アルコール性脂肪肝炎(NASH)による肝硬変の方は、参加者が集まったため、募集を終了とさせていただきました。皆様、ご協力の程、ありがとうございました。
また、この治験では肝硬変の症状が進行して、肝性脳症や腹水がたまるなどの症状がでている方(非代償性肝硬変といいます)、又は過去にそのような症状の治療を行った方を対象としております。
但し、重篤な肝硬変と診断された場合(Child-Pugh分類がグレードC)にはご協力いただくことはできません。
Webアンケートから応募24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
治験実施医療機関所在地
北海道
北海道札幌市北区
北海道札幌市手稲区
東北
岩手県紫波郡
福島県郡山市
関東
東京都港区
東京都文京区
東京都板橋区
東京都目黒区
神奈川県横浜市南区
神奈川県川崎市高津区
埼玉県川越市
埼玉県入間郡毛呂山町
千葉県市川市
千葉県印西市
茨城県稲敷郡
中部
長野県長野市
長野県松本市
静岡県伊豆の国市・静岡県浜松市
愛知県名古屋市昭和区
岐阜県岐阜市
福井県福井市
近畿
大阪府大阪市阿倍野区・大阪府大阪市住吉区・大阪府大阪市中央区
奈良県橿原市
兵庫県西宮市
中国・四国
山口県下関市
愛媛県東温市
九州
福岡県福岡市東区
佐賀県佐賀市
長崎県長崎市
※2026年1月5日時点の治験実施医療機関所在地です。各医療機関で治験の定員が決まっています。お早めにご応募ください。
※治験実施医療機関の名称は、ご応募の後、来院する事が決まった患者さまへのみご説明しています。
本治験の概要
治験参加のスケジュール
約1年間(52週間)が治験参加期間となります。
最初の24週間は1週間に2回通院し、毎回約3~4時間かけて治験薬の点滴注射を受けていただきます。
その後は観察期間となり、治験薬の投与はなく検査の為に3回程度ご来院いただくことになります。
医師の判断により来院回数が増える場合もあります。
これらのスケジュールにすべてご参加いただくことになります。
患者さんが支払う費用と受け取る費用について
治験薬は無償で提供されます。
治験に係る検査、画像診断の費用は製薬企業が負担いたしますので患者さまのお支払いはありません。
治験にご協力いただいたことで患者さまに発生する負担(交通費や時間的な制約など)を軽減する目的で規定の負担軽減費が支払われます。
Webアンケートから応募24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
治験に参加するまでの流れ

- STEP.
- ◆Webアンケートから応募する
Webアンケートにお答えください。
入力いただいた内容を確認後、治験お問合せセンターより
お電話させていただきます。
◆電話で応募する
肝硬変治験お問合せセンターにお電話ください。

- STEP.
- お電話にて参加条件を確認させていただきます。
※Webアンケートにてご応募いただいた場合、アンケート内容と重複する質問をさせていただく場合がございますがご了承ください。
この時点でこの治験で定められている参加条件に合致しないことがわかった場合には、治験実施医療機関をご案内することなく終了となる場合がありますので予めご了承ください。
お電話で確認できる範囲の参加条件を満たしていた場合には、治験実施医療機関の初回来院をご案内いたします。
この治験の定員の都合で、初回来院までしばらくお待ちいただくことや、お待ちいただいても初回来院をすることなく終了してしまう可能性があることをご承知おきください。

- STEP.
- 治験実施医療機関で治験の詳細な説明を受けて参加するかどうかをじっくり検討してください。
参加しなくても患者さまには何の不利益もありません。
また参加を始めた後でも患者さまの自由な意思により理由を問わず自由に参加を中止することができます。
尚、治験実施医療機関に来院した後でも、治験で定められた参加条件に合わない場合や、医師の判断、定員の都合等様々な理由により治験にご参加いただけない、または治験参加を途中でお断りする場合があることをご理解、ご了承ください。
Webアンケートから応募24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
お問い合わせ
ご不明な点や、不安に思っていることなどがございましたら「治験お問合せセンター」へお気軽にお電話でご相談ください。
尚、「治験お問合せセンター」では回答できる範囲が限られていることをご理解の上お問い合わせください。
大原薬品工業株式会社は、「治験お問合せセンター」を特定非営利活動法人ニューイングに委託しております。
0120-800-739 【受付時間】平日9:00~17:00(土・日・祝日・年末年始を除く)
【開設期間】2026年10月までを予定(治験の定員に達した場合は早期に終了いたします)
肝硬変で線維化してしまった肝臓を改善するお薬の開発が始まっています。

主な参加条件
- 18歳~79歳でB型肝炎、C型肝炎、非アルコール性脂肪肝炎(NASH)による肝硬変と診断された方
※非アルコール性脂肪肝炎(NASH)による肝硬変の方は、参加者が集まったため、募集を終了とさせていただきました。皆様、ご協力の程、ありがとうございました。
- 最寄りの治験実施医療機関に週2回(点滴時間:3~4時間)計24週間の通院ができる方
- Child-Pugh分類がグレードB(中等度:7~9点)の方(わからなくてもご応募いただけます)
- かかりつけ医から、診療情報提供書を発行していただける方
※今回の治験では肝硬変の原因がB型肝炎、C型肝炎、非アルコール性脂肪肝炎(NASH)であると診断された方に限定させていただいております。
非アルコール性脂肪肝炎(NASH)による肝硬変の方は、参加者が集まったため、募集を終了とさせていただきました。皆様、ご協力の程、ありがとうございました。
また、この治験では肝硬変の症状が進行して、肝性脳症や腹水がたまるなどの症状がでている方(非代償性肝硬変といいます)、又は過去にそのような症状の治療を行った方を対象としております。
但し、重篤な肝硬変と診断された場合(Child-Pugh分類がグレードC)にはご協力いただくことはできません。
非アルコール性脂肪肝炎(NASH)による肝硬変の方は、参加者が集まったため、募集を終了とさせていただきました。皆様、ご協力の程、ありがとうございました。
また、この治験では肝硬変の症状が進行して、肝性脳症や腹水がたまるなどの症状がでている方(非代償性肝硬変といいます)、又は過去にそのような症状の治療を行った方を対象としております。
但し、重篤な肝硬変と診断された場合(Child-Pugh分類がグレードC)にはご協力いただくことはできません。
Webアンケートから応募
24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
治験実施医療機関所在地
北海道
北海道札幌市北区
北海道札幌市手稲区
東北
岩手県紫波郡
福島県郡山市
関東
東京都港区
東京都文京区
東京都板橋区
東京都目黒区
神奈川県横浜市南区
神奈川県川崎市高津区
埼玉県川越市
埼玉県入間郡毛呂山町
千葉県市川市
千葉県印西市
茨城県稲敷郡
中部
長野県長野市
長野県松本市
静岡県伊豆の国市・静岡県浜松市
愛知県名古屋市昭和区
岐阜県岐阜市
福井県福井市
近畿
大阪府大阪市阿倍野区・大阪府大阪市住吉区・大阪府大阪市中央区
奈良県橿原市
兵庫県西宮市
中国・四国
山口県下関市
愛媛県東温市
九州
福岡県福岡市東区
佐賀県佐賀市
長崎県長崎市
※2026年1月5日時点の治験実施医療機関所在地です。各医療機関で治験の定員が決まっています。お早めにご応募ください。
※治験実施医療機関の名称は、ご応募の後、来院する事が決まった患者さまへのみご説明しています。
本治験の概要
治験参加のスケジュール
約1年間(52週間)が治験参加期間となります。
最初の24週間は1週間に2回通院し、毎回約3~4時間かけて治験薬の点滴注射を受けていただきます。
その後は観察期間となり、治験薬の投与はなく検査の為に3回程度ご来院いただくことになります。
医師の判断により来院回数が増える場合もあります。
これらのスケジュールにすべてご参加いただくことになります。
最初の24週間は1週間に2回通院し、毎回約3~4時間かけて治験薬の点滴注射を受けていただきます。
その後は観察期間となり、治験薬の投与はなく検査の為に3回程度ご来院いただくことになります。
医師の判断により来院回数が増える場合もあります。
これらのスケジュールにすべてご参加いただくことになります。
患者さんが支払う費用と受け取る費用について
治験薬は無償で提供されます。
治験に係る検査、画像診断の費用は製薬企業が負担いたしますので患者さまのお支払いはありません。
治験にご協力いただいたことで患者さまに発生する負担(交通費や時間的な制約など)を軽減する目的で規定の負担軽減費が支払われます。
治験に係る検査、画像診断の費用は製薬企業が負担いたしますので患者さまのお支払いはありません。
治験にご協力いただいたことで患者さまに発生する負担(交通費や時間的な制約など)を軽減する目的で規定の負担軽減費が支払われます。
Webアンケートから応募
24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
治験に参加するまでの流れ

- STEP.
- ◆Webアンケートから応募する
Webアンケートにお答えください。
入力いただいた内容を確認後、治験お問合せセンターより
お電話させていただきます。
◆電話で応募する
肝硬変治験お問合せセンターにお電話ください。

- STEP.
- お電話にて参加条件を確認させていただきます。
※Webアンケートにてご応募いただいた場合、アンケート内容と重複する質問をさせていただく場合がございますがご了承ください。
この時点でこの治験で定められている参加条件に合致しないことがわかった場合には、治験実施医療機関をご案内することなく終了となる場合がありますので予めご了承ください。
お電話で確認できる範囲の参加条件を満たしていた場合には、治験実施医療機関の初回来院をご案内いたします。
この治験の定員の都合で、初回来院までしばらくお待ちいただくことや、お待ちいただいても初回来院をすることなく終了してしまう可能性があることをご承知おきください。

- STEP.
- 治験実施医療機関で治験の詳細な説明を受けて参加するかどうかをじっくり検討してください。
参加しなくても患者さまには何の不利益もありません。
また参加を始めた後でも患者さまの自由な意思により理由を問わず自由に参加を中止することができます。
尚、治験実施医療機関に来院した後でも、治験で定められた参加条件に合わない場合や、医師の判断、定員の都合等様々な理由により治験にご参加いただけない、または治験参加を途中でお断りする場合があることをご理解、ご了承ください。
Webアンケートから応募
24時間受付
電話で応募・問い合わせ0120-800-739
平日9:00~17:00(土・日・祝日・年末年始を除く)
お問い合わせ
ご不明な点や、不安に思っていることなどがございましたら「治験お問合せセンター」へお気軽にお電話でご相談ください。
尚、「治験お問合せセンター」では回答できる範囲が限られていることをご理解の上お問い合わせください。
尚、「治験お問合せセンター」では回答できる範囲が限られていることをご理解の上お問い合わせください。
大原薬品工業株式会社は、「治験お問合せセンター」を特定非営利活動法人ニューイングに委託しております。
0120-800-739
【受付時間】平日9:00~17:00(土・日・祝日・年末年始を除く)
【開設期間】2026年10月までを予定(治験の定員に達した場合は早期に終了いたします)
